en
names in breadcrumbs

Der Waschbärspulwurm (Baylisascaris procyonis) ist eine bei Waschbären häufige Fadenwurmart. Sie wurde in den USA auch im Darm von Hunden nachgewiesen. Generell ist diese Art – auch in Europa – als potenzieller Erreger von Larva migrans visceralis bei Tieren und Menschen von Interesse.
Im Darm eines ausgewachsenen Waschbären können 200 Waschbärspulwürmer leben, ohne dass das Wirtstier dadurch wesentlich beeinträchtigt wird. Daraus resultieren Millionen von mikroskopisch kleinen Wurmeiern im Bärenkot, die mitunter jahrelang überleben können. Die Eier selbst sind harmlos, aber innerhalb der nächsten 2–4 Wochen entwickeln sich aus den Eiern die infektiösen Larven. Als Zwischenwirte fungieren in erster Linie kleine Tiere, Nager und Vögel, die später auch als Nahrung für den Waschbären dienen. Im Darm des Zwischenwirts schlüpfen die Larven aus den Eiern, können die Darmwand durchdringen und sich in unterschiedlichen Organen oder Gewebe einnisten. Das Nervensystem kann schwer geschädigt werden und zu Lethargie, Koordinations- und Gleichgewichtsstörungen, Schädigungen der Augen und des Gehirns, Koma und bei stärkerem Befall auch zum Tod des Wirtstieres führen. Größere Haustiere und Säugetiere als Fehlwirte können den Befall auch folgenlos überstehen. Die Aufnahme der Larven erfolgt durch Verzehr der lebenden oder verendeten Zwischenwirtstiere. Der Waschbärspulwurm erreicht nur im Waschbären sein ausgewachsenes Stadium.
Der Waschbärspulwurm (Baylisascaris procyonis) ist eine bei Waschbären häufige Fadenwurmart. Sie wurde in den USA auch im Darm von Hunden nachgewiesen. Generell ist diese Art – auch in Europa – als potenzieller Erreger von Larva migrans visceralis bei Tieren und Menschen von Interesse.
Im Darm eines ausgewachsenen Waschbären können 200 Waschbärspulwürmer leben, ohne dass das Wirtstier dadurch wesentlich beeinträchtigt wird. Daraus resultieren Millionen von mikroskopisch kleinen Wurmeiern im Bärenkot, die mitunter jahrelang überleben können. Die Eier selbst sind harmlos, aber innerhalb der nächsten 2–4 Wochen entwickeln sich aus den Eiern die infektiösen Larven. Als Zwischenwirte fungieren in erster Linie kleine Tiere, Nager und Vögel, die später auch als Nahrung für den Waschbären dienen. Im Darm des Zwischenwirts schlüpfen die Larven aus den Eiern, können die Darmwand durchdringen und sich in unterschiedlichen Organen oder Gewebe einnisten. Das Nervensystem kann schwer geschädigt werden und zu Lethargie, Koordinations- und Gleichgewichtsstörungen, Schädigungen der Augen und des Gehirns, Koma und bei stärkerem Befall auch zum Tod des Wirtstieres führen. Größere Haustiere und Säugetiere als Fehlwirte können den Befall auch folgenlos überstehen. Die Aufnahme der Larven erfolgt durch Verzehr der lebenden oder verendeten Zwischenwirtstiere. Der Waschbärspulwurm erreicht nur im Waschbären sein ausgewachsenes Stadium.
Baylisascaris procyonis, also known by the common name of raccoon roundworm, is a roundworm nematode, found ubiquitously in raccoons, the definitive hosts. It is named after H. A. Baylis, who studied them in the 1920s–30s, and Greek askaris (intestinal worm).[1] Baylisascaris larvae in paratenic hosts can migrate, causing visceral larva migrans (VLM). Baylisascariasis as the zoonotic infection of humans is rare, though extremely dangerous due to the ability of the parasite's larvae to migrate into brain tissue and cause damage. Concern for human infection has been increasing over the years due to urbanization of rural areas resulting in the increase in proximity and potential human interaction with raccoons.[2]
The potential for human infection was noted in 1969 by Paul C. Beaver, who studied infected mice, and the first case was reported 15 years later.[2] Human infection with B. procyonis has been relatively rare, with about 30 cases reported since 1980. However, disease caused by this parasite can be extremely dangerous, causing death or severe symptoms. Reported disease has primarily afflicted children and almost all cases were a result of the ingestion of contaminated soil or feces.[3] Even with treatment, prognosis is poor and patients in nearly all cases experience permanent neurological damage. Infection of the eyes may result in permanent visual damage and loss. The common antihelmintic medicines are able to treat adult worms living in the intestines, but are less effective against migrating larvae.[3] Aggressive and early treatment with corticosteroids and albendazole have in a few instances resulted in complete recoveries.[4] It is possible that human infection is more common than diagnosed and most cases do not reach a clinical stage.[5][6] Antibodies to B. procyonis have been found in otherwise healthy individuals, suggesting subclinical infections.[5][7]
In North America, B. procyonis infection rates in raccoons are very high, being found in around 70% of adult raccoons and 90% of juvenile raccoons.[6] Transmission occurs similarly to other roundworm species, through the fecal-oral route. Eggs are produced by the worm while in the intestine, and the released eggs will mature to an infective state externally in the soil. When an infected egg is ingested, the larvae will hatch and enter the intestine. Transmission of B. procyonis may also occur through the ingestion of larvae found in infected tissue.[6]
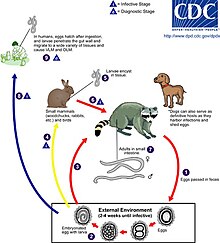
An adult worm lives and reproduces in the intestine of its definitive host, the raccoon. The female worm can produce between 115,000–179,000 eggs per day. Eggs are excreted along with feces, and become infective in the soil after 2–4 weeks. If ingested by another raccoon, the life cycle repeats. However, if these eggs are ingested by an intermediate host (small mammals, birds) the larvae of B. procyonis will penetrate the gut wall of the host and migrate into tissues. Larvae tend to migrate to the brain, cause damage, and affect the behaviour of the intermediate host, making it an easier prey for raccoons. Reproduction does not occur in these intermediate hosts; however, if a raccoon preys on an infected paratenic host, the encysted larvae can become adults in the raccoon and the cycle resumes.[2]
Laboratory and clinical diagnosis can be challenging: there is no commercially available serologic test in the United States, and although identification of larvae in tissue or specimens is confirmatory, this is not always possible or practical.[4]
Diagnosis of B. procyonis is through identification of larvae in tissue examination. Diagnosis requires forehand knowledge along with understanding and recognition of larval morphologic characteristics, including ability to distinguish between a number of possible other parasites, including Toxocara canis, Toxocara cati, Ascaris lumbricoides, and among species of Gnathostoma, Angiostrongylus, and Ancylostoma.[6] Distinguishing features of B. procyonis larvae in tissue are its relatively large size (60 μ) and prominent single lateral alae. Sometimes serologic testing is used as supportive evidence, although no commercial serologic test is currently available. Other diagnosis methods include: brain biopsy, neuroimaging, electroencephalography, differential diagnoses among other laboratory tests.[3]
Human Baylisascariasis is under-recognized, as the knowledge of the clinical illness is still a bit unclear. This could be because of the difficulty of diagnosing the illness. As small numbers of larvae can cause severe disease, and larvae occur randomly in tissue, a biopsy usually fails to include larvae and therefore leads to negative results. The identification of the morphologic characteristics takes practice and experience and may not be accurately recognized or could be misidentified. The fact that no commercial serologic test exists for the diagnosis of B. procyonis infection makes the diagnosis and treatment more difficult.[6]
Educating the public about the dangers of contact with raccoons or their feces is the most important preventive step.[3]
Parents should encourage their children to practice good hygiene; Hand-washing after outdoor play or contact with animals is very important. Fences can be used to prevent raccoons from visiting homes, garbage, or yards for food. Keeping raccoons as pets is strongly discouraged. Raccoon latrines in and around homes should be checked for and cleaned as soon as possible. Boiling water, steam-cleaning, flaming, or fire are highly effective and are easily accessible means to decontaminate household things or areas. Materials contaminated by B.procyonis should be incinerated. Contaminated areas can be cleaned with a xylene-ethanol mixture. Common chemical disinfectants are not effective against B.procyonis eggs. Disinfectants like 20% bleach (1% sodium hypochlorite) wash away the eggs but do not kill them. Since treatment is not very effective, the best way to escape this parasite is to practice the prevention methods.[3]
B. procyonis is found abundantly in its definitive host, the raccoon. The parasite has been found to have the ability to infect more than 90 kinds of wild and domestic animals.[6] Many of these animals act as paratenic hosts and the infection results in the penetration of the gut wall by the larvae and subsequent invasion of tissue, resulting in severe disease. In animals, it is the most common cause of larva migrans.[3] The paratenic host, however, cannot shed infective eggs, as the larva will not complete its life cycle until it makes its way into a raccoon. Raccoons are solitary but will frequently defecate in communal areas known as raccoon latrines. These latrines are an abundant source of B. procyonis eggs, which can remain viable for years.[3] Raccoons therefore are important in maintaining the parasite, providing a source of infection for humans and other animals.[3]
The white-footed mouse (Peromyscus leucopus) among other small rodents are considered common intermediate hosts.[8] Migration patterns of rodents can explain the spread of Baylisascaris to multiple locations and the subsequent infection of humans who may come into contact with eggs shed by infected raccoons. The mice may be infected as a result of contact with raccoon latrines. Foraging upon food contaminated with traces of raccoon feces can also lead to exposure to B. procyonis eggs. Rodents are easily found in many areas with human population which increases the risk of transmission.[9] The increase in the raccoon population (and inevitably B. procyonis) has become a major factor for the number of extirpations the Allegheny woodrat (Neotoma magister) has suffered in recent decades.[10][11]
B. procyonis has become a concern for its potential use as an agent of bioterrorism. The fact that this parasite's eggs are easy to acquire, able to live for years, extremely resistant to many disinfectants, and cause serious infections in humans with poor treatment options could make it a dangerous weapon.[3] Community water supplies are easily susceptible to contamination due to the lack of filtration and treatment methods to get rid of the eggs.[12]
Baylisascaris procyonis, also known by the common name of raccoon roundworm, is a roundworm nematode, found ubiquitously in raccoons, the definitive hosts. It is named after H. A. Baylis, who studied them in the 1920s–30s, and Greek askaris (intestinal worm). Baylisascaris larvae in paratenic hosts can migrate, causing visceral larva migrans (VLM). Baylisascariasis as the zoonotic infection of humans is rare, though extremely dangerous due to the ability of the parasite's larvae to migrate into brain tissue and cause damage. Concern for human infection has been increasing over the years due to urbanization of rural areas resulting in the increase in proximity and potential human interaction with raccoons.
Baylisascaris procyonis es una especie de nemátodo de la familia de los ascáridos causante de larva migrans cerebral. Se trata de una afección emergente en Europa y en expansión ya que antes sólo existía en América. Su llegada a Europa está ligada a la introducción de mapaches (Procyon lotor) para la industria peletera en 1936. El primer caso en Europa en hombre tuvo lugar en 1991.
La hembra produce millones de huevos al día durante meses o incluso años. Afecta a gallináceas, roedores, lagomorfos, etc. El hospedador definitivo es el mapache, al que le produce una afección neurológica grave: parálisis, volteo, ceguera, ataxia. En algunos animales produce un síndrome neurológico mortal. Se contrae por ingestión de comida, agua o tierra infectada con huevos de esta especie.
Baylisascaris procyonis es una especie de nemátodo de la familia de los ascáridos causante de larva migrans cerebral. Se trata de una afección emergente en Europa y en expansión ya que antes sólo existía en América. Su llegada a Europa está ligada a la introducción de mapaches (Procyon lotor) para la industria peletera en 1936. El primer caso en Europa en hombre tuvo lugar en 1991.
Baylisascaris procyonis, communément appelé « ascaris du raton laveur », est un nématode qui est omniprésent chez les ratons laveurs et dont les larves causent la toxocarose chez les hôtes intermédiaires par lesquels elles migrent. L'infection de l'homme par ce parasite est une anthropozoonose rare mais fort dangereuse, car la larve du parasite peut passer dans le cerveau[1] et causer des dommages. La crainte de cette infection de l'homme a augmenté au fil des ans parce que l'urbanisation des régions rurales augmente la proximité des ratons laveurs et la possibilité d'interaction entre eux et l'homme[2].
En Amérique du Nord, le taux d'infection des ratons laveurs par B. procyonis est très élevé : il est d'environ 70 % chez les adultes et de 90 % chez les jeunes[3]. La transmission se produit de façon semblable à celle des autres nématodes, par la voie fécale et orale. Les œufs sont produits par le ver dans l'intestin et, une fois excrétés, parviennent à un stade infectieux dans le sol. Lorsque l'œuf infectieux est ingéré, la larve éclot et entre dans l'intestin. La transmission de B. procyonis peut aussi se produire par l'ingestion de tissus infectés de larves[3].
B. procyonis se trouve abondamment chez son hôte définitif, le raton laveur. On a constaté que ce parasite était capable d'infecter plus de 90 sortes d'animaux sauvages et domestiques[3]. Nombre de ces derniers servent d'hôtes intermédiaires, et l'infection permet aux larves de percer la paroi abdominale pour envahir les tissus de l'hôte et causer de graves maladies. Chez les animaux, elle est la cause la plus courante de larva migrans[4]. Le raton laveur joue un rôle important dans le cycle de vie de la maladie. C'est un animal solitaire, mais il défèque souvent dans des sites préférentiels appelés latrines[5]. Ces latrines sont une source abondante d'œufs de B. procyonis, qui demeurent viables plusieurs années[4]. Le raton laveur est donc important pour la sauvegarde du parasite et représente une source d'infection pour l'homme et d'autres animaux[4].
Le ver adulte, ver allongé de 12 (mâle) à 23 (femelle) cm de long, effilé aux extrémités, qui ressemble beaucoup à l'ascaris du chien, vit et se reproduit dans l'intestin de son hôte définitif, le raton laveur[6]. La femelle peut pondre de 115 000 à 179 000 œufs par jour. Ils sont excrétés dans les matières fécales et deviennent infectieux dans le sol après deux à quatre semaines. S'ils sont ingérés par un autre raton laveur, le cycle de vie se répète ; mais s'ils le sont par un hôte intermédiaire (un petit mammifère ou un oiseau), les larves de B. procyonis percent la paroi intestinale et migrent dans les tissus de l'hôte. Elles ont tendance à migrer jusqu'au cerveau, causent des dommages et altèrent le comportement de l'hôte intermédiaire, ce qui en fait une proie plus facile pour le raton laveur. Le nématode ne se reproduit pas dans l'hôte intermédiaire (le chien a toutefois été reconnu pour être un porteur occasionnel de vers fertiles[5]), mais si le raton laveur fait sa proie de cet hôte, les larves enkystées peuvent alors atteindre le stade adulte, et le cycle reprend[2].
La possibilité d'une infection de l'homme est signalée par Paul C. Beaver en 1969 à la suite de l'étude de souris infectées, et le premier cas d'infection est signalé 15 ans plus tard[2]. L'infection de l'homme par B. procyonis est relativement rare : on n'a signalé qu'environ 13 cas depuis 1980. Cependant, la maladie causée par ce parasite peut être extrêmement dangereuse et causer de graves symptômes, voire la mort. Les cas signalés de maladie étaient surtout des enfants, et presque tous résultaient de l'ingestion de sol ou d'excréments contaminés[4]. Sur ces 13 cas, 5 ont été mortels, et les autres se sont soldés par de graves séquelles neurologiques. Le pronostic est sombre même en cas de traitement. Les anthelminthiques courants sont efficaces contre les vers adultes vivant dans l'intestin, mais sont moins efficaces contre les larves en migration. Des études sur animaux ont montré que le traitement est plus efficace avant que les larves n'atteignent le cerveau, mais la migration vers ce dernier se produit déjà trois jours après l'ingestion, ce qui réduit de beaucoup les chances de succès d'un traitement[4].
B. procyonis est un nématode préoccupant, car il pourrait servir d'agent de bioterrorisme. Le fait que ses œufs sont faciles à acquérir, capables de vivre plusieurs années et extrêmement résistants à la chaleur et à de nombreux désinfectants et qu'ils causent chez l'homme de graves infections dont les traitements possibles sont peu efficaces pourrait en faire une arme dangereuse[4].
Baylisascaris procyonis, communément appelé « ascaris du raton laveur », est un nématode qui est omniprésent chez les ratons laveurs et dont les larves causent la toxocarose chez les hôtes intermédiaires par lesquels elles migrent. L'infection de l'homme par ce parasite est une anthropozoonose rare mais fort dangereuse, car la larve du parasite peut passer dans le cerveau et causer des dommages. La crainte de cette infection de l'homme a augmenté au fil des ans parce que l'urbanisation des régions rurales augmente la proximité des ratons laveurs et la possibilité d'interaction entre eux et l'homme.
Baylisascaris procyonis, (conhecido como lombriga do guaxinim) é um nematóide encontrado de forma ubíqua em guaxinins, os hospedeiros definitivos. Nomeado conforme H. A. Baylis, que os estudou nas décadas de 1920 e 1930.[1] As larvas de Baylisascaris em hospedeiros paratênicos podem migrar, causando larva migrans visceral. A Baylisascaríase como infecção zoonótica em humanos é rara, embora extremamente perigosa devido à capacidade das larvas do parasita migrarem para o tecido cerebral e causar danos permanentes. A preocupação com a infecção humana tem vindo a aumentar ao longo dos anos devido à urbanização das zonas rurais, resultando no aumento da proximidade e potencial de interação humana com guaxinins.[2]
O potencial de infecção humana foi observado em 1969 por Paul C. Beaver, que estudou camundongos infectados, e o primeiro caso foi relatado 15 anos depois.[2] A infecção humana com B. procyonis tem sido relativamente rara, com cerca de 30 casos relatados desde 1980. No entanto, a doença causada por este parasita pode ser extremamente perigosa, causando morte ou sintomas graves. A doença relatada atingiu principalmente crianças e quase todos os casos foram resultado da ingestão de solo ou fezes contaminados.[3] Mesmo com o tratamento, o prognóstico é ruim e os pacientes em quase todos os casos apresentam danos neurológicos permanentes. A infecção dos olhos pode resultar em danos e perda visual permanente. Os medicamentos anti-helmínticos comuns são capazes de tratar vermes adultos que vivem nos intestinos, mas são menos eficazes contra a migração de larvas.[3] O tratamento agressivo e precoce com corticosteroides e albendazol resultou, em alguns casos, em recuperações completas.[4] É possível que a infecção humana seja mais comum do que diagnosticada e a maioria dos casos não atinge um estágio clínico. Anticorpos para B. procyonis foram encontrados em indivíduos saudáveis, sugerindo infecções subclínicas.[5][6][7]
Na América do Norte, as taxas de infecção por B. procyonis em guaxinins são muito altas, sendo encontradas em cerca de 70% de guaxinins adultos e 90% de guaxinins juvenis.[6] A transmissão ocorre de forma semelhante a outras espécies de lombrigas, através da via fecal-oral. Os ovos são produzidos pelo verme no intestino, e os ovos liberados amadurecem para um estado infeccioso externamente no solo. Quando um ovo infectado é ingerido, as larvas eclodem e entram no intestino. A transmissão de B. procyonis também pode ocorrer pela ingestão de larvas encontradas no tecido infectado.[6]
Um verme adulto vive e se reproduz no intestino de seu hospedeiro definitivo, o guaxinim. O verme fêmea pode produzir entre 115.000 e 179.000 ovos por dia. Os ovos são excretados junto com as fezes e tornam-se infectantes no solo após 2 a 4 semanas. Se ingerido por outro guaxinim, o ciclo de vida se repete. No entanto, se esses ovos forem ingeridos por um hospedeiro paratênico (pequenos mamíferos, aves), as larvas de B. procyonis penetrarão na parede intestinal do hospedeiro e migrarão para os tecidos. As larvas tendem a migrar para o cérebro, causar danos e afetar o comportamento do hospedeiro intermediário, tornando-o uma presa mais fácil para os guaxinins. A reprodução não ocorre nesses hospedeiros paratênicos; no entanto, se um guaxinim ataca um hospedeiro paratênico infectado, as larvas encistadas podem se tornar adultas no guaxinim e o ciclo recomeça.[2]
O diagnóstico laboratorial e clínico pode ser desafiador: não há teste sorológico comercialmente disponível nos Estados Unidos e, embora a identificação de larvas em tecidos ou espécimes seja confirmatória, isso nem sempre é possível ou prático.[4] O diagnóstico de B. procyonis é feito através da identificação das larvas no exame tecidual. O diagnóstico requer conhecimento prévio, juntamente com a compreensão e reconhecimento das características morfológicas larvais, incluindo a capacidade de distinguir entre vários outros parasitas possíveis, incluindo Toxocara canis, Toxocara cati, Ascaris lumbricoides e entre espécies de Gnathostoma, Angiostrongylus e Ancylostoma.[6] As características distintivas das larvas de B. procyonis no tecido são seu tamanho relativamente grande (60 μ). Às vezes, o teste sorológico é usado como evidência de suporte, embora nenhum teste sorológico comercial esteja disponível atualmente. Outros métodos de diagnóstico incluem: biópsia cerebral, neuroimagem, eletroencefalografia, diagnósticos diferenciais entre outros exames laboratoriais.[3] A Baylisascaríase humana é pouco reconhecida, pois o conhecimento da doença clínica ainda é um pouco obscuro. Isso pode ser devido à dificuldade de diagnosticar a doença. Como um pequeno número de larvas pode causar doença grave e as larvas ocorrem aleatoriamente no tecido, uma biópsia geralmente não inclui larvas e, portanto, leva a resultados negativos. A identificação das características morfológicas requer prática e experiência e pode não ser reconhecida com precisão ou pode ser identificada erroneamente. O fato de não existir nenhum teste sorológico comercial para o diagnóstico da infecção por B. procyonis dificulta o diagnóstico e o tratamento.[6]
Educar o público sobre os perigos do contato com guaxinins ou suas fezes é o passo preventivo mais importante. Os pais devem incentivar seus filhos a praticar uma boa higiene; Lavar as mãos após brincar ao ar livre ou contato com animais é muito importante. As cercas podem ser usadas para evitar que os guaxinins visitem casas, lixo ou quintais em busca de comida.[3] Manter guaxinins como animais de estimação é fortemente desencorajado. As latrinas de guaxinim dentro e ao redor das casas devem ser verificadas e limpas o mais rápido possível. Água fervente, limpeza a vapor ou fogo são altamente eficazes e são meios de fácil acesso para descontaminar coisas ou áreas domésticas. Materiais contaminados por Baylisascaris procyonis devem ser incinerados. As áreas contaminadas podem ser limpas com uma mistura de xileno-etanol. Desinfetantes químicos comuns não são eficazes contra ovos de B.procyonis. Desinfetantes como 20% de alvejante (1% de hipoclorito de sódio) lavam os ovos, mas não os matam. Como o tratamento não é muito eficaz, a melhor maneira de escapar desse parasita é praticar os métodos de prevenção.[3]
B. procyonis é encontrado abundantemente em seu hospedeiro definitivo, o guaxinim. Descobriu-se que o parasita tem a capacidade de infectar mais de 90 tipos de animais selvagens e domésticos. Muitos desses animais atuam como hospedeiros paratênicos e a infecção resulta na penetração da parede intestinal pelas larvas e subsequente invasão do tecido, resultando em doença grave. Em animais, é a causa mais comum de larva migrans.[3] O hospedeiro paratênico, no entanto, não pode liberar ovos infecciosos, pois a larva não completará seu ciclo de vida até chegar ao guaxinim. Guaxinins são solitários, mas frequentemente defecam em áreas comuns conhecidas como latrinas de guaxinim. Essas latrinas são uma fonte abundante de ovos de B. procyonis, que podem permanecer viáveis por anos. Os guaxinins, portanto, são importantes na manutenção do parasita, fornecendo uma fonte de infecção para humanos e outros animais. O camundongo de patas brancas (Peromyscus leucopus) entre outros pequenos roedores são considerados hospedeiros paratênicos comuns.[9] Os padrões de migração de roedores podem explicar a disseminação de Baylisascaris para vários locais e a subsequente infecção de humanos que podem entrar em contato com ovos de guaxinins infectados. Os camundongos podem ser infectados como resultado do contato com latrinas de guaxinins. Forragear alimentos contaminados com vestígios de fezes de guaxinim também pode levar à exposição a ovos de B. procyonis. Os roedores são facilmente encontrados em muitas áreas com população humana, o que aumenta o risco de transmissão.
B. procyonis tornou-se uma preocupação por seu uso potencial como agente de bioterrorismo.[10] O fato de os ovos desse parasita serem fáceis de adquirir, capazes de viver por anos, extremamente resistentes a muitos desinfetantes e causar infecções graves em humanos com poucas opções de tratamento pode torná-lo uma arma perigosa.[3] O abastecimento de água da comunidade é facilmente suscetível à contaminação devido à falta de métodos de filtragem e tratamento para se livrar dos ovos.
Baylisascaris procyonis, (conhecido como lombriga do guaxinim) é um nematóide encontrado de forma ubíqua em guaxinins, os hospedeiros definitivos. Nomeado conforme H. A. Baylis, que os estudou nas décadas de 1920 e 1930. As larvas de Baylisascaris em hospedeiros paratênicos podem migrar, causando larva migrans visceral. A Baylisascaríase como infecção zoonótica em humanos é rara, embora extremamente perigosa devido à capacidade das larvas do parasita migrarem para o tecido cerebral e causar danos permanentes. A preocupação com a infecção humana tem vindo a aumentar ao longo dos anos devido à urbanização das zonas rurais, resultando no aumento da proximidade e potencial de interação humana com guaxinins.
アライグマ回虫(アライグマかいちゅう、アライグマ蛔虫、学名:Baylisascaris procyonis)とは、アライグマを宿主とする回虫の1種。
成虫は円筒形で、長さが雄 9-11cm 、雌 20-22cm あり、アライグマの小腸に寄生する。人間に感染した場合には、脳に達して急性障害を発生させ死に至らしめる。1日あたり10万個を超える膨大な卵を体外へ放出することで知られ、飼育環境下で発生した場合の周辺環境、特に人体への影響は大きい。
アメリカ合衆国では、1981年以降に12例の発症が報告され、うち3名(いずれも小児)が死亡している。発生例自体希少であるため、看過されている可能性はある。日本での発症例、野生アライグマからの検出例ともには報告されたことはない(動物園等で飼育されているアライグマからの検出事例はある)。アライグマに関して言えば、特定外来生物による生態系等に係る被害の防止に関する法律により輸入、飼育が制限されており、アライグマが原因となる拡大は懸念される状況にはないが、飼育されているウサギから発見されたこともあり、今後は、アライグマ以外での動物においての発生状況及び輸入個体のチェックが必要になると考えられている。