pt-BR
nomes no trilho de navegação

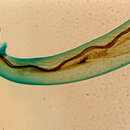
Angiostrongylus cantonensis was initially found in the lungs of rodents in China. It was given little notice since it was not yet found in humans. In 1944, the first case of A. cantonensis in a human was found. A young adult worm was in the cerebrospinal fluid of a young boy in Taiwan who had come in for treatment for meningitis. Since then, many cases have been linked to eosinophilic meningoencephalitis. Even though its symptoms are similar to other diseases, if it shows up in an area that didn't have it before, research will be prompted to start to see if the worm has reached that area. If symptoms show up in an area that is known to have the worm, then the worm will be the first suspect.
Nematodes within the Secernentea have phasmids, which are unicellular glands. Phasmids likely function as chemoreceptors. Females may produce pheromones to attract males.
Nematodes in general have papillae, setae and amphids, which are the main sense organs. Setae detect motion (mechanoreceptors), while amphids detect chemicals (chemoreceptors).
Communication Channels: tactile ; chemical
Other Communication Modes: pheromones
Perception Channels: tactile ; chemical
The worms molt before becoming adults, two molts occuring before they hatch from the eggs. Most all adult structures except certain reproductive parts are found in the young just after hatching. As adults, the worms will not molt, but can grow in size.
Angiostrongylus cantonensis has a complex life cycle that involves intermediate, paratenic, and definitive hosts as well as several larval stages before becoming an adult. Adults are found in the right ventricles of hearts and the pulmonary arteries. The females release their eggs in these arteries. They are carried to the lungs, and within the capillaries here they embryonate. The thin-shelled egg breaks open and the first larval stage hatches. The larvae break through the alveoli and move up the trachea, where they wait to be swallowed and then expelled in the feces.
The intermediate host starts eating the fecal matter, also ingesting the parasitic larvae. There is some development in the intermediate host, but not to sexual maturity. The larvae develop into the 3rd stage in the molluscan muscle tissue. A parantenic host such as a frog or fish may eat the intermediate host, where the larvae survive in their muscle but no development occurs. The larvae enters the definitive host either by ingestion of the intermediate host, ingestion of paratenic host, or ingestion of material that contains the slimy path that a slug or snail leaves behind. Larvae may escape the intermediate host and be present on that trail.
Once inside the intestine of the definitive host, the larvae go through obligatory migration through the central nervous system via bloodstream to the brain and spinal cord. They leave the capillaries and start wandering randomly through the tissues. At the same time, they reach the fifth stage larvae. When the larvae reach the surface of the brain or spinal cord, they penetrate the veins to reenter the circulatory system. The larvae end up at the pulmonary arteries where they mature into adults in about six weeks. However, some larvae wander to other places in the body and mature there. Common places are in the central nervous system, the meninges, and the eyes.
Angiostrongylus cantonensis is the primary cause of human eosinophilic meningoencephalitis in many parts of the Indo-Pacific region. The hosts become infected when the third stage larva is ingested. Humans get severe headaches, stiff necks, clouded consciousness, meningeal irritations, and extensive tissue damage from wandering worms in the brain. Eosinophil counts are increased in peripheral blood and spinal fluid, and lymphocyte counts are increased in the cerebrospinal fluid. The final results of these symptoms lead to neural disorders, paralysis of 5th cranial nerve, comas, and even death.
Dead worms that are present in the blood stream can cause inflammatory responses. Immune responses are evoked by dead worms and cause the destruction of brain and spinal cord cells. However, symptoms are so vague that they can be mistaken for a variety of other parasitic diseases. With this delay in correct diagnosis, dead worms can be worse than live worms.
Negative Impacts: injures humans (causes disease in humans )
Angiostrongylus cantonensis is not specific for either definitive or intermediate hosts. The requirement is that the intermediate host must be an invertebrate while the definitive is a terrestrial mammal. Paratenic hosts, where the parasites don't develop to the next stage, can be either invertebrate or vertebrate. The definitive hosts for Angiostrongylus cantonensis are usually rodents from the genus g. Rattus, with some main ones being Rattus norvegicus and Rattus rattus. Angiostrongylus cantonensis can survive in humans and monkeys as well.
The main intermediate hosts include slugs and snails. Paratenic hosts include anything that eats the mollusks. Some main ones include terrestrial planarians and crabs, fresh-water shrimp and frogs, toads, marine fish, and sea snakes. However, recent evidence indicates it may be intolerant of salinity, so marine species may be questionable as hosts.
Ecosystem Impact: parasite
Species Used as Host:
Angiostrongylus cantonensis has a simple mouth and no buccal cavity. Pharyngeal glands and intestinal epithelium produce digestive enzymes, and feed on the body fluids of its hosts. Extracellular digestion begins within the intestine, and the digestive cycle is completed intracellularly.
As an endoparasite, Angiostrongylus cantonensis is usually found in the pulmonary arteries and in the right ventricle of the heart. The larvae are found circulating in the blood, spinal fluid, cerebrospinal fluid, or in the blood vessels of the brain and the meninges. Angiostrongylus cantonensis is mainly found in rodents, especially rats, which are the definitive hosts. The worm has also been able to survive and sexually mature in other mammals including humans and monkeys.
Animal Foods: body fluids
Primary Diet: carnivore (Eats body fluids)
Angiostrongylus cantonensis was discovered in China. Since then it has been found in Australia, the southwestern Pacific including Hawaii, South and southeast Asia, Madagascar, Japan, Taiwan, Egypt, Ivory Coast of Africa, India, Samoa, Fiji, Cuba, the Caribbean, Puerto Rico, and Southeastern USA. Angiostrongylus cantonensis probably originated in eastern Asia, but because of its large dispersal as a result of human activity, there is no way to be sure.
Biogeographic Regions: nearctic ; palearctic ; oriental ; ethiopian ; neotropical ; australian ; oceanic islands (Native )
Other Geographic Terms: cosmopolitan
Angiostrongylus cantonensis is not specific for either definitive or intermediate hosts. The requirement is that the intermediate host must be an invertebrate while the definitive is a terrestrial mammal. Paratenic hosts, where the parasites don't develop to the next stage, can be either invertebrate or vertebrate. The definitive hosts for Angiostrongylus cantonensis are usually rodents from the genus Rattus, with some main ones being Rattus norvegicus and Rattus rattus. Angiostrongylus cantonensis can survive in humans and monkeys as well. Two cases of monkeys dying from complications of eosinophilic meningoencephalitis in zoos were attributed to their contact with snails serving as intermediate hosts.
The main intermediate hosts include slugs and snails. Achatina fulica, or the African giant land snail, can contain thousands of third-stage larvae. Although it's not the major intermediate host, this particular snail is important because it may be a primary reason why Angiostrongylus cantonensis has spread. This snail is considered a delicacy in several regions and typically eaten raw. With the amount of larvae in one Achatina fulica, A. cantonensis can easily be dispersed to new areas.
Paratenic hosts include anything that eats the mollusks. Some main ones include terrestrial planarians and crabs, fresh-water shrimp and frogs, toads, marine fish, and sea snakes. However, recent evidence indicates it may be intolerant of salinity, so marine species may be questionable as hosts.
Habitat Regions: temperate ; tropical ; terrestrial ; saltwater or marine ; freshwater
Terrestrial Biomes: forest ; rainforest
Aquatic Biomes: lakes and ponds; rivers and streams; temporary pools; coastal
Wetlands: marsh ; swamp
Other Habitat Features: urban ; suburban ; agricultural ; riparian ; estuarine ; intertidal or littoral
Lifespan and growth to the next parasitic larval stage depends on what host is infected. In paratenic hosts, the larval may not develop to the next stage.
As a nematode, A. cantonensis is cylindrical, and has a cuticle with three main outer layers made of collagen and other compounds. The outer layers are non-cellular and are secreted by the epidermis. The cuticle layer protects nematodes so they can invade digestive tracts of animals. The worms molt four times, the first two before hatching, and then before their adult stage.
As a member of the Secernentea, A. cantonensis has a specialized tubular excretory system system with three canals. The canals are arranged to from an "H".
Angiostrongylus cantonensis is a flimsy and slender worm with a simple mouth and no lips or buccal cavity. The bursa, a structure used to clasp females when copulating, is small and dorsal lobe is not present. The males have long and slender spicules which are almost equal in length and form. The gubernaculum, used to guide spicules when mating, is present but is not immediately noticeable.
There are obvious differences between male and female A. cantonensis. The males are 15.9 to 19 mm in length, while the females can grow 21 to 25 mm in length. Females are easily distinguished from males by the noticeable barber-pole appearance in their bodies. This is actually the interweaving of the intestine and uterine tubules. Females have a vulva, which is located 0.2 mm in front of the anus.
Range length: 15.9 to 25 mm.
Other Physical Features: ectothermic ; homoiothermic; bilateral symmetry
Sexual Dimorphism: female larger; sexes shaped differently
These parasites are usually not preyed on directly, but are ingested from host to host. Larval mortality is high as most of the parasites do not reach appropriate hosts.
Females may produce a pheromone to attract males. The male coils around a female with his curved area over the female genital pore. The gubernaculum, made of cuticle tissue, guides spicules which extend through the cloaca and anus. Males use spicules to hold the females during copulation. Nematode sperm are amoeboid-like and lack flagella.
Average age at sexual or reproductive maturity (female): 6 weeks.
Average age at sexual or reproductive maturity (male): 6 weeks.
Key Reproductive Features: gonochoric/gonochoristic/dioecious (sexes separate); sexual ; fertilization (Internal ); oviparous
Parental Investment: pre-fertilization
The nematode (roundworm) Angiostrongylus cantonensis, the Rat Lungworm, is the most common cause of human eosinophilic meningitis, a meningoencephalitis characterized by eosinophils in the cerebrospinal fluid. Humans are accidental hosts for these parasites. Most cases of eosinophilic meningitis have been reported from Southeast Asia and the Pacific Basin, although the infection is spreading to many other areas of the world, including Africa and the Caribbean.
Adult A. cantonensis live in the pulmonary arteries of rats. The females lay eggs that hatch, yielding first-stage larvae, in the terminal branches of the pulmonary arteries. The first-stage larvae migrate to the pharynx, are swallowed, and pass in the feces. They penetrate, or are ingested by, an intermediate host (snail or slug). After two molts, third-stage larvae are produced, which are infective to mammalian hosts. When the mollusk is ingested by the definitive host, the third-stage larvae migrate to the brain where they develop into young adults. The young adults return to the venous system and then to the pulmonary arteries, where they become sexually mature. A variety of animals can act as paratenic (transport) hosts: after ingesting the infected snails, they carry the third-stage larvae, which can resume their development when the paratenic host is ingested by a definitive host. Humans can acquire the infection by eating raw or undercooked snails or slugs infected with the parasite; they may also acquire the infection by eating raw produce that contains a small snail or slug, or part of one. There is some question regarding whether or not larvae can exit the infected mollusks in slime (which might be infective to humans if ingested, for example, on produce). The disease can also be acquired by ingestion of contaminated or infected paratenic animals (crabs, freshwater shrimps). In humans, juvenile worms migrate to the brain, or rarely to the lungs, where they ultimately die.
Der Ratten-Lungenwurm (Angiostrongylus cantonensis) ist ein Parasit, dessen Hauptwirt Ratten sind, in deren Lungen er lebt. Als Zwischenwirt dienen verschiedene Landschnecken und Krabben. Experimentell sind auch Meeresfische infizierbar, allerdings wird angenommen, dass die Larven keine große Resistenz gegen Salzwasser aufweisen. Auch Menschen können durch den Parasiten infiziert werden – etwa, wenn sie infizierte, nicht durchgegarte Schnecken essen.
Ursprüngliches Verbreitungsgebiet ist der Pazifische Raum und Südostasien. Allerdings hat sich der Wurm seither auch in folgenden Gebieten ausgebreitet: Australien, Melanesien, Mikronesien und Polynesien, Neukaledonien, den Philippinen, Rarotonga, Saipan, Sumatra, Taiwan sowie Tahiti. Ab den 60er Jahren gab es Meldungen aus Kambodscha, Guam, Hawaii, Java, Thailand, Sarawak, Vietnam und den Neuen Hebriden (Vanuatu). Die Erstbeschreibung stammt aus China. Weiter wurde der Parasit auch in die Karibik eingeschleppt. Es wurden einige Exemplare in Ratten aus Kuba, Puerto Rico, der Dominikanischen Republik und Jamaika gefunden. Ein Einzelfall einer Infektion durch das Verschlucken einer unbekannten Schneckenart wurde in Australien[1] festgestellt. Forscher warnten 2019 vor dem Verzehr unzureichend gekochte Schneckengerichte auf Mallorca; 2018 war der Ratten-Lungenwurm auf Mallorca in zwei Igeln gefunden worden.[2][3]
Der Parasit weist die typische Nematodenform auf. Die Haut besteht aus drei Kollagenschichten, welche es dem Parasit ermöglichen, das Immunsystem des Wirtes zu umgehen. Die männlichen Tiere besitzen eine Art Beutel, mit dem sich das Männchen am Weibchen festklammert. Es besteht ein Geschlechtsdimorphismus, die Weibchen werden 25 bis 33 mm lang, die Männchen hingegen nur 15 bis 19 mm. Der Körper ist von einem s-förmigen schwarzen Band durchzogen, das den Darm und den Uterus darstellt.
Die Entwicklung beginnt in der Ratte, in der die adulten Weibchen leben. Diese halten sich in der rechten Herzkammer und den Lungenarterien auf. Die Eier werden dort freigesetzt. Sie wandern in die Kapillaren der Lunge, wo aus den Eiern die Larven schlüpfen, welche im 1. Larvenstadium durch die Alveolen ausbrechen und ausgehustet werden. Einige werden wieder geschluckt und nun im 2. Larvenstadium über den Kot ausgeschieden.
Der Zwischenwirt nimmt nun über den Rattenkot die Larven auf. Diese entwickeln sich in ihm zum 3. Larvenstadium. Ein als Nebenwirt dienender Frosch oder Fisch kann in Folge durch Fressen des Zwischenwirtes die Larven ebenfalls aufnehmen. Hier findet jedoch keine Entwicklung mehr statt.
Der Hauptwirt infiziert sich, indem er den Zwischenwirt oder den Nebenwirt frisst. Allerdings dringt die Larve in der Schnecke auch aktiv nach außen, sodass in der Schleimspur infektiöse Larven vorhanden sind, die von der Ratte (dem Hauptwirt) auch aufgenommen werden. Dort wandern sie entlang des Nervensystems über den Blutstrom ins Gehirn. Vom Gehirn aus verbreiten sie sich im ganzen Körper, verlassen über die Kapillare den Blutstrom und treten ins Gewebe über. Dort entwickelt sich das 5. Larvenstadium. Dieses sucht erneut das Gehirn auf und lässt sich danach hauptsächlich in den Lungenarterien nieder, aber auch andere Stellen wie das Auge oder die Hirnhäute oder das Zentralnervensystem werden befallen. In circa 6 Wochen entwickelt sich aus der Larve das adulte Tier. Nach mehreren Häutungen und der Paarung werden erneut Eier ins Blut abgegeben.
Menschen können sich über kontaminierte Nahrung, auch den Zwischenwirten, infizieren und bei den Infizierten kann der Parasit eine eosinophile Meningoenzephalitis (Entzündung des Gehirns und der Hirnhäute) auslösen. Klinische Symptome einer Infektion mit dem Ratten-Lungenwurm sind starke Kopfschmerzen, Meningismus und neurologische Ausfälle. Die Erkrankung kann bis zum Koma und Tod fortschreiten.[4] Besonders gefährdet sind Personen mit Immunschwäche (z. B. Schwangere, HIV-Infizierte, Personen mit angeborenen Immunschwächen). Im Liquor cerebrospinalis der Betroffenen finden sich typischerweise hohe Zahlen an Eosinophilen.
Zwischen 2007 und 2017 infizierten sich 82 Personen im US-Bundesstaat Hawaii, mehrere starben.[2]
Der Ratten-Lungenwurm (Angiostrongylus cantonensis) ist ein Parasit, dessen Hauptwirt Ratten sind, in deren Lungen er lebt. Als Zwischenwirt dienen verschiedene Landschnecken und Krabben. Experimentell sind auch Meeresfische infizierbar, allerdings wird angenommen, dass die Larven keine große Resistenz gegen Salzwasser aufweisen. Auch Menschen können durch den Parasiten infiziert werden – etwa, wenn sie infizierte, nicht durchgegarte Schnecken essen.
Angiostrongylus cantonensis is a parasitic nematode (roundworm) that causes angiostrongyliasis, the most common cause of eosinophilic meningitis in Southeast Asia and the Pacific Basin.[2] The nematode commonly resides in the pulmonary arteries of rats, giving it the common name rat lungworm.[3] Snails are the primary intermediate hosts, where larvae develop until they are infectious.
Humans are incidental hosts of this roundworm, and may become infected through ingestion of larvae in raw or undercooked snails or other vectors, or from contaminated water and vegetables.[4] The larvae are then transported via the blood to the central nervous system, where they are the most common cause of eosinophilic meningitis, a serious condition that can lead to death or permanent brain and nerve damage.[5] Angiostrongyliasis is an infection of increasing public health importance, as globalization contributes to the geographic spread of the disease.[6][7]
First described by Chinese parasitologist Hsin-Tao Chen (1904–1977) in 1935, after examining Cantonese rat specimens,[1] the nematode Angiostrongylus cantonensis was identified in the cerebrospinal fluid of a patient with eosinophilic meningitis by Nomura and Lim in Taiwan in 1944. They noted that raw food eaten by the patient may have been contaminated by rats.
During her time working at the Queensland Institute for Medical Research (QIMR), Australian entomologist Mabel Josephine Mackerras catalogued the history of rat lungworm. This enabled later research to identify it as the etiological agent of eosinophilic meningitis in Pacific Islanders, leading researchers to name the species after her.[8]

A. cantonensis is a helminth of the phylum Nematoda, order Strongylida, and superfamily Metastrongyloidea. Nematodes are roundworms characterized by a tough outer cuticle, unsegmented bodies, and a fully developed gastrointestinal tract. The order Strongylida includes hookworms and lungworms. Metastrongyloidea are characterized as 2-cm-long,[9] slender, threadlike worms that reside in the lungs of the definitive host.[10] Angiostrongylus costaricensis is a closely related worm that causes intestinal angiostrongyliasis in Central and South America.
Following World War II, A. cantonensis spread throughout Southeast Asia and Western Pacific Islands, including Australia, Melanesia, Micronesia, and Polynesia. Cases were soon reported in New Caledonia, the Philippines, Rarotonga, Saipan, Sumatra, Taiwan, and Tahiti. In the 1960s, even more cases were reported from the region from locations such as Cambodia, Guam, Hawaii, Java, Thailand, Sarawak, Vietnam, and Vanuatu.[11]
In 1961, an epidemiological study of eosinophilic meningitis in humans was conducted by Rosen, Laigret, and Bories, who hypothesized that the parasite causing these infections was carried by fish. However, Alicata noted that raw fish was consumed by large numbers of people in Hawaii without apparent consequences, and patients presenting with meningitis symptoms had a history of eating raw snails or prawns in the weeks before presenting with symptoms. This observation, along with epidemiology and autopsy of infected brains, confirmed A. cantonensis infection in humans as the cause of the majority of eosinophilic meningitis cases in Southeast Asia and the Pacific Islands.[12]
Since then, cases of A. cantonensis infestations have appeared in American Samoa, Australia, Hong Kong, Bombay, Fiji, Hawaii, Honshu, India, Kyushu, New Britain, Okinawa, Ryukyu Islands, Western Samoa, and most recently mainland China. Other sporadic occurrences of the parasite in its rat hosts have been reported in Cuba, Egypt, Louisiana, Madagascar, Nigeria, and Puerto Rico.[11]
In 2013, A. cantonensis was confirmed present in Florida, USA, where its range and prevalence are expanding.[13] In 2018, a case was found in a New Yorker who had visited Hawaii.[14]
In recent years, the parasite has been shown to be proliferating at an alarming rate due to modern food-consumption trends and global transportation of food products. Scientists are calling for a more thorough study of the epidemiology of A. cantonensis, stricter food-safety policies, and the increase of knowledge on how to properly consume products commonly infested by the parasite, such as snails and slugs that act as intermediate hosts or those that act as paratenic hosts, such as fish, frogs, or freshwater prawns.[15][16][17] Ingestion of food items that can be contaminated by the mucus excretions of intermediate or paratenic hosts, such as snails and slugs, or by the feces of rats that act as definitive hosts, can lead to infection of A. cantonensis.[18] The most common route of infection of A. cantonesis in humans is by ingestion of either intermediate or paratenic hosts of the larvae.[19] Unwashed fruits and vegetables, especially romaine lettuce, can be contaminated with snail and slug mucus or can result in accidental ingestion of these intermediate and paratenic hosts. These items need to be properly washed and handled to prevent accidental ingestion of A. cantonensis larvae or the larvae-containing hosts.[20] The best mechanism of prevention of A. cantonesis outbreak is to institute an aggressive control of snail and slug population, proper cooking of intermediate and paratenic hosts such as fish, freshwater prawn, frogs, molluscs, and snails along with proper food-handling techniques.[21] The common prevention techniques for diarrheal illness are very effective in preventing A. cantonensis infection.[22] Not much is known about why it targets the brain in humans, but a chemically induced chemotaxis has been implicated recently. Acetylcholine has been previously reported to enhance motility of this worm via nicotinic acetylcholine receptors.[23] Experimental assays in animal models are needed to validate a chemically induced chemotaxis by use of anticholinergic drugs to prevent cerebral infection following infections by A. cantonesis.[24]
Intermediate hosts of larvae of for A. cantonensis include:
Definitive hosts of A. cantonensis include wild rodents, especially the brown rat (Rattus norvegicus) and the black rat (Rattus rattus).[25]
Paratenic hosts of A. cantonensis include the predatory land flatworm Platydemus manokwari and the amphibians, Bufo asiaticus, Rana catesbeiana, Polypedates leucomystax and Fejervarya limnocharis.[29]
In 2004, a captive yellow-tailed black cockatoo (Calyptorhynchus funereus) and two free-living tawny frogmouths (Podargus strigoides) suffering neurological symptoms were shown to have the parasite. They were the first avian hosts discovered for the organism.[34] In 2018, in Mallorca two North African hedgehogs with signs of acute neurological disease were found to have A. cantonensis in their brains, one of them with a gravid female.[35] It was the first report of hedgehogs as hosts of Angiostrongylus.[35]
The Hawaiʻi Dept. of Health states that fresh water opihi can carry the parasite, as well as other aquatic organisms such as prawns, frogs, and water monitor lizards.[36] House pets may interact with A. cantonensis-carrying animals yet not well studied. Cats are known to carry and spread feline lungworm in rat and snail interactions.[37]
The presence of parasitic worms burrowed in the neural tissue of the human central nervous system (CNS) causes complications. All of the following result in damage to the CNS:
Although the clinical disease caused by Angiostrongylus invasion into the CNS is commonly referred to as "eosinophilic meningitis", the actual pathophysiology is of a meningoencephalitis with invasion not just of the meninges, or superficial lining of the brain, but also deeper brain tissue. Initial invasion through the lining of the brain, the meninges, may cause a typical inflammation of the meninges and a classic meningitis picture of headache, stiff neck, and often fever. The parasites subsequently invade deeper into the brain tissue, causing specific localizing neurological symptoms depending on where in the brain parenchyma they migrate. Neurologic findings and symptoms wax and wane as initial damage is done by the physical in-migration of the worms and secondary damage is done by the inflammatory response to the presence of dead and dying worms. This inflammation can lead in the short term to paralysis, bladder dysfunction, visual disturbance, and coma and in the long term to permanent nerve damage, mental retardation, nerve damage, permanent brain damage, or death.[38]
Eosinophilic meningitis is commonly defined by the increased number of eosinophils in the cerebrospinal fluid (CSF). In most cases, eosinophil levels rise to 10 or more eosinophils per μl in the CSF, accounting for at least 10% of the total CSF leukocyte (white blood cell) count.[39] The chemical analysis of the CSF typically resembles the findings in "aseptic meningitis" with slightly elevated protein levels, normal glucose levels, and negative bacterial cultures. Presence of a significantly decreased glucose on CSF analysis is an indicator of severe meningoencephalitis and may indicate a poor medical outcome. Initial CSF analysis early in the disease process may occasionally show no increase of eosinophils, only to have classical increases in eosinophils in subsequent CSF analysis. Caution should be advised in using eosinophilic meningitis as the only criterion for diagnosing angiostrongylus infestation in someone with classic symptoms, as the disease evolves with the migration of the worms into the CNS.
Eosinophils are specialized white blood cells of the granulocytic cell line, which contain granules in their cytoplasm. These granules contain proteins that are toxic to parasites. When these granules degranulate, or break down, chemicals are released that combat parasites such as A. cantonensis. Eosinophils, which are located throughout the body, are guided to sites of inflammation by chemokines when the body is infested with parasites such as A. cantonensis. Once at the site of inflammation, type 2 cytokines are released from helper T cells, which communicate with the eosinophils, signaling them to activate. Once activated, eosinophils can begin the process of degranulation, releasing their toxic proteins in the fight against the foreign parasite.
According to a group case study, the most common symptoms in mild eosinophilic meningitis tend to be headache (with 100% of people in the study suffering from this symptom), photophobia or visual disturbance (92%), neck stiffness (83%), fatigue (83%), hyperesthesias (75%), vomiting (67%), and paresthesias (50%).[40][22] Incubation period is often 3 weeks, but can be 3–36 days[11] and even 80 days.[41]
Possible clinical signs and symptoms of mild and severe eosinophilic meningitis are:
The severity and clinical course of Angiostrongylus disease depends significantly on the ingested load of third-stage larvae,[43] creating great variability from case to case, making clinical trials difficult to design, and effectiveness of treatments difficult to discern. Typical conservative medical management including analgesics and sedatives provide minimal relief for the headaches and hyperesthesias. Removing cerebrospinal fluid at regular 3- to 7-day intervals is the only proven method of significantly reducing intracranial pressure and can be used for symptomatic treatment of headaches.[44] This process may be repeated until improvement is shown.[39] There is growing evidence of moderate quality that suggests corticosteroid therapy using prednisolone[45] or dexamethasone[46] has beneficial effect in treating the CNS symptoms related to A. cantonensis infections.[47][48] Although early research did not show treatment with antihelminthic agents (parasite-killing drugs) such as thiobendazole or albendazole effective in improving the clinical course of the illness,[49][40] a number of recent studies from Thailand and China show that the combination of glucocorticoids and antihelminthics is safe and decreases the duration of headaches and the number of patients who had significant headache.[46][45][50][51] Although the addition of antihelminthic agents for management of A. cantonensis infection has a theoretic risk of precipitating a neurologic crisis by releasing an overwhelming load of antigens through simultaneous death of the larvae,[44] no study has shown this to exist in the clinical setting.[47][46][51][45] Additionally, the failure to kill parasites before they attempt to migrate out of the CNS increases the risk of mechanical damage by migrating larvae. Although combination therapy using albendazole and prednisolone has no significant advantage compared to treatment using prednisolone alone in mild cases,[52] the treatment with antihelminthics is demonstrably safe and may have significant benefit for patients with high parasite loads at risk for permanent disability or death.[38]
The diagnosis of disease caused by A. cantonensis infestation is often difficult and relies heavily on the history of a likely ingestion of a commonly infested host and the presence of typical features of the disease. The presumptive diagnosis is particularly strong when eosinophilic meningoencephalitis can be confirmed. The diagnosis of eosinophilic meningitis can be arrived at through detection of elevated cranial pressure and increased numbers of eosinophils. The diagnosis of the cause of eosinophilic meningitis and the presence of A. cantonensis is remarkably more difficult. A spinal tap, or a sample of CSF, must be taken to search for A. cantonensis worms or larvae. A. cantonensis is undetectable in the CSF of more than half of the infected individuals. Current methods of detecting specific antigens associated with A. cantonensis are also unreliable. Consequently, alternative approaches to detect antigen-antibody reactions are being explored, such as immuno-PCR.[53] A rapid dot-blot ELISA test is also available for quick, effective, and economical on-site diagnosis of A. cantonensis.[54]
{{cite web}}: CS1 maint: others (link) Angiostrongylus cantonensis is a parasitic nematode (roundworm) that causes angiostrongyliasis, the most common cause of eosinophilic meningitis in Southeast Asia and the Pacific Basin. The nematode commonly resides in the pulmonary arteries of rats, giving it the common name rat lungworm. Snails are the primary intermediate hosts, where larvae develop until they are infectious.
Humans are incidental hosts of this roundworm, and may become infected through ingestion of larvae in raw or undercooked snails or other vectors, or from contaminated water and vegetables. The larvae are then transported via the blood to the central nervous system, where they are the most common cause of eosinophilic meningitis, a serious condition that can lead to death or permanent brain and nerve damage. Angiostrongyliasis is an infection of increasing public health importance, as globalization contributes to the geographic spread of the disease.
Angiostrongylus cantonensis es una especie de parásito nematodo que causa angiostrongiliasis, la causa más común de meningitis eosinofílica en el sureste de Asia y la cuenca del Pacífico.[2] El nematodo por lo general reside en las arterias pulmonares de ratas, de allí su nombre común lombriz pulmonar de las ratas.[3] Los caracoles son los hospedadores primarios intermedios, donde se desarrollan las larvas hasta que pueden infectar.
Los seres humanos son huéspedes incidentales de esta lombriz intestinal y pueden infectarse por la ingestión de larvas en caracoles u otros vectores crudos o poco cocidos, o por agua y verduras contaminadas.[4] Luego, las larvas se transportan a través de la sangre al sistema nervioso central, donde son la causa más común de meningitis eosinofílica, una afección grave que puede provocar la muerte o daño cerebral y nervioso permanente.[5] La angiostrongiliasis es una infección de creciente importancia para la salud pública, ya que la globalización contribuye a la propagación geográfica de la enfermedad.[6][7]
Fue inicialmente identificado por el destacado parasitólogo chino Hsin-Tao Chen en 1935, luego de examinar especímenes de rata,[1] el nematodo Angiostrongylus cantonensis fue identificado en el fluido cerebroespinal de un paciente con meningitis eosinofílica por Nomura y Lim en Taiwán en 1944. Ellos notaron que era posible que la comida cruda ingerida por el paciente estuviera contaminada por ratas. En 1955, Mackerass y Sanders identificaron el ciclo vital de la lombriz en las ratas, definiendo a los caracoles y babosas como hospedadores intermedios, y notando que la transmisión ocurría a través de la sangre, cerebro y pulmones de las ratas.
Angiostrongylus cantonensis es una especie de parásito nematodo que causa angiostrongiliasis, la causa más común de meningitis eosinofílica en el sureste de Asia y la cuenca del Pacífico. El nematodo por lo general reside en las arterias pulmonares de ratas, de allí su nombre común lombriz pulmonar de las ratas. Los caracoles son los hospedadores primarios intermedios, donde se desarrollan las larvas hasta que pueden infectar.
Los seres humanos son huéspedes incidentales de esta lombriz intestinal y pueden infectarse por la ingestión de larvas en caracoles u otros vectores crudos o poco cocidos, o por agua y verduras contaminadas. Luego, las larvas se transportan a través de la sangre al sistema nervioso central, donde son la causa más común de meningitis eosinofílica, una afección grave que puede provocar la muerte o daño cerebral y nervioso permanente. La angiostrongiliasis es una infección de creciente importancia para la salud pública, ya que la globalización contribuye a la propagación geográfica de la enfermedad.
Angiostrongylus cantonensis est une espèce de nématodes, dont l'adulte parasite les artères pulmonaires du rat et dont les larves au stade 3 peuvent évoluer chez l'espèce humaine en donnant la méningite angiostrongylienne à éosinophiles.
A. cantonensis est un nématode parasite du genre Angiostrongylus(1-4). Les femelles mesurent 21 à 25 mm de long, tandis que les mâles mesurent 16 à 19 mm de long. Les vers matures vivent dans les artères pulmonaires des rats et pondent des œufs fertilisés qui se transforment en larves de premier stade. Ces larves migrent d'abord vers la trachée et sont ensuite dégluties et éliminées dans les excréments. Elles demeurent viables et infectieuses dans les excréments ou l'eau douce pendant plusieurs semaines. Le cycle de vie n'est complété que si ces larves sont ingérées par un mollusque (limaçons ou limaces), qui agit en tant qu'hôte intermédiaire. Environ deux semaines plus tard, les larves atteignent le stade de maturité, soit le troisième stade, c'est-à-dire qu'elles deviennent alors infectieuses pour le restant de la vie des mollusques. Les crevettes, les poissons, les crabes, les grenouilles, les planaires terrestres ou les varans peuvent dévorer les mollusques infectés et servir d'hôtes paraténiques. Les rongeurs ingèrent les mollusques ou les hôtes paraténiques et deviennent alors infectés. Chez l'humain (cul-de-sac épidémiologique), l'infection est causée par l'ingestion de la chair crue d'hôtes paraténiques ou intermédiaires contaminés ou par l'ingestion de légumes contaminés par des larves de troisième stade.
Le rat élimine avec ses matières fécales les larves du 1er stade, qui doivent obligatoirement séjourner chez un mollusque - hôte intermédiaire - pour aboutir à la larve du 3e stade, seule infectieuse pour l'hôte définitif. Différents mollusques terrestres et aquatiques peuvent jouer ce rôle, parfois relayés par certains crustacés d'eau douce qui servent d'« hôte paraténique » (crevettes, crabes de mangrove...) C'est en mangeant crus ces mollusques et crustacés, qui entrent dans la composition de diverses préparations culinaires traditionnelles, que l'homme s'infecte le plus souvent. Des crudités mal lavées cachant une limace infectée ou de l'eau de puits contaminés par des larves après la mort de mollusques parasités ont été incriminées dans les contaminations accidentelles. Libérées par la digestion, les larves franchissent la muqueuse intestinale et migrent par voie sanguine vers le cerveau où elles s'installent.
A. cantonensis existe à l'intérieur de la ceinture intertropicale : très répandu en Extrême-Orient, en Australie, dans toutes les îles du Pacifique, de l'Océan Indien et à Madagascar. Dans les années 1980, il a été signalé en Afrique, mais la contamination humaine y semble exceptionnelle, et dans les Caraïbes, où il est responsable de cas humains sporadiques, notamment à Cuba et en Martinique [2] , et de contamination de voyageurs, notamment en Jamaïque et en République Dominicaine, destinations fortement touristiques.
L'espèce a été décrite en 1935[1].
Les larves au stade 3 peuvent évoluer chez l'espèce humaine en donnant la méningite angiostrongylienne à éosinophiles.
Simple curiosité nosologique dans les régions où la contamination est purement accidentelle, la méningite angiostrongylienne devient endémo-épidémique dans toutes celles où cette contamination est liée à des coutumes alimentaires dangereuses (Thaïlande, Polynésie...).
Toutefois, l'issue n'est pas nécessairement heureuse. Selon divers titres de presse[3], en 2010, un patient australien serait devenu paraplégique après avoir ingéré une limace porteuse d'Angiostrongylus cantonensis. Il est décédé en 2018.
Le diagnostic repose sur la constatation de l'éosinophilie rachidienne, la notion de contexte épidémiologique et le mode d'évolution.
Le traitement est purement symptomatique.
Angiostrongylus cantonensis est une espèce de nématodes, dont l'adulte parasite les artères pulmonaires du rat et dont les larves au stade 3 peuvent évoluer chez l'espèce humaine en donnant la méningite angiostrongylienne à éosinophiles.
Angiostrongylus cantonensis è un nematode parassita che causa l'angiostrongiliasi, la causa più comune di meningite eosinofila nell'Asia sud-orientale e nel bacino del Pacifico. Il nematode risiede comunemente nelle arterie polmonari dei ratti, da cui anche il nome comune di "laringe di ratto". Le lumache sono i principali ospiti intermedi, dove le larve si sviluppano fino a diventare infettive.
Gli esseri umani sono ospiti incidentali di questo nematode e possono essere infettati attraverso l'ingestione di larve in lumache crude o poco cotte o altri vettori o da acqua e verdure contaminate. Le larve vengono poi trasportate attraverso il sangue al sistema nervoso centrale, dove sono la causa più comune di meningite eosinofila, una condizione grave che può portare alla morte o danni permanenti al cervello e ai nervi. Angiostrongyliasis è un'infezione di crescente importanza per la salute pubblica, poiché la globalizzazione contribuisce alla diffusione geografica della malattia.
Descritto per la prima volta dal parassitologo cinese Hsin-Tao Chen (1904-1977) nel 1935, dopo aver esaminato esemplari di ratto cantonese, il nematode Angiostrongylus cantonensis è stato identificato nel liquido cerebrospinale di un paziente con meningite eosinofila di Taiwan nel 1944. Fu notato che il cibo crudo mangiato dal paziente poteva essere stato contaminato dai ratti. Nel 1955, Mackerass e Sanders identificarono il ciclo vitale del verme nei ratti, definendo le lumache come ospiti intermedi e notando il percorso di trasmissione attraverso il sangue, il cervello e i polmoni nei ratti.
Dopo la seconda guerra mondiale, l'A. cantonensis si diffuse in tutto il Sud-est asiatico e nelle isole del Pacifico occidentale, tra cui Australia, Melanesia, Micronesia e Polinesia. Casi furono presto segnalati in Nuova Caledonia, nelle Filippine, a Rarotonga, a Saipan, a Sumatra, a Taiwan e a Tahiti. Negli anni '60, sono stati segnalati ancora altri casi da località come Cambogia, Guam, Hawaii, Giava, Tailandia, Sarawak, Vietnam e le Nuove Ebridi (Vanuatu).
Nel 1961, uno studio epidemiologico sulla meningite eosinofila nell'uomo fu condotto da Rosen, Laigret e Bories, i quali ipotizzarono che il parassita che causa queste infezioni fosse trasportato dai pesci. Tuttavia, Alicata ha osservò che il pesce crudo era consumato da un gran numero di persone alle Hawaii senza conseguenze apparenti, e i pazienti che presentavano sintomi di meningite avevano una storia di consumo di lumache o gamberi crudi nelle settimane precedenti alla presentazione dei sintomi. Questa osservazione, insieme all'epidemiologia e all'autopsia del cervello infetto, confermo l'infezione da A. cantonensis negli esseri umani come causa della maggior parte dei casi di meningite eosinofila nell'Asia sud-orientale e nelle isole del Pacifico.
Da allora, casi di infestazioni di A. cantonensis sono apparsi nelle Samoa Americane, Australia, Hong Kong, Bombay, Fiji, Hawaii, Honshu, India, Kyushu, Nuova Britannia, Okinawa, Isole Ryukyu, Samoa occidentali e, più recentemente, in Cina. Altri episodi sporadici del parassita nei suoi ospiti di ratti sono stati segnalati a Cuba, in Egitto, in Louisiana, in Madagascar, in Nigeria, a New Orleans e a Porto Rico.
Nel 2013, A. cantonensis è stato confermato in Florida, negli Stati Uniti, dove la sua presenza è in espansione. Nel 2018, un caso fu trovato in un newyorkese che aveva visitato le Hawaii. Negli ultimi anni, il parassita ha dimostrato di proliferare a un ritmo allarmante a causa delle moderne tendenze del consumo alimentare e del trasporto globale di prodotti alimentari. Gli scienziati hanno a più riprese chiesto uno studio più approfondito dell'epidemiologia dell'A. cantonensis nonché politiche di sicurezza alimentare più severe e l'aumento delle conoscenze su come consumare correttamente i prodotti comunemente infestati dal parassita, come lumache e lumache che fungono da ospiti intermedi o quelli che fungono da ospiti paratenici, come pesci, rane o gamberi d'acqua dolce.
L'ingestione di alimenti che possono essere contaminati dalle escrezioni di muco di ospiti intermedi o paratenici, come le lumache o dalle feci di ratti che fungono da ospiti definitivi, può portare a infezioni di A. cantonensis. La via più comune di infezione di A. cantonensis nell'uomo è l'ingestione di ospiti intermedi o paratenici delle larve. Frutta e verdura non lavate, in particolare la lattuga, possono essere contaminate da muco di lumaca e lumaca o possono causare l'ingestione accidentale di questi ospiti intermedi e paratenici. Questi articoli devono essere adeguatamente lavati e maneggiati per evitare l'ingestione accidentale delle larve di A. cantonensis o degli ospiti contenenti larve. Il miglior meccanismo di prevenzione dell'epidemia di A. cantonesis è quello di istituire un controllo aggressivo della popolazione di lumache e lumache, una corretta cottura di ospiti intermedi e paratenici come pesci, gamberi d'acqua dolce, rane, molluschi e lumache insieme ad alimenti adeguati.
Le tecniche di prevenzione comuni per la malattia diarrea sono molto efficaci nel prevenire l'infezione da A. cantonensis. Non si sa molto sul motivo per cui colpisce il cervello negli esseri umani, ma una chemiotassi chimicamente indotta è stata recentemente osservata. Si è osservato inoltre che l'acetilcolina migliora la motilità di questo verme attraverso i recettori nicotinici dell'acetilcolina.
Angiostrongylus cantonensis è un nematode parassita che causa l'angiostrongiliasi, la causa più comune di meningite eosinofila nell'Asia sud-orientale e nel bacino del Pacifico. Il nematode risiede comunemente nelle arterie polmonari dei ratti, da cui anche il nome comune di "laringe di ratto". Le lumache sono i principali ospiti intermedi, dove le larve si sviluppano fino a diventare infettive.
Gli esseri umani sono ospiti incidentali di questo nematode e possono essere infettati attraverso l'ingestione di larve in lumache crude o poco cotte o altri vettori o da acqua e verdure contaminate. Le larve vengono poi trasportate attraverso il sangue al sistema nervoso centrale, dove sono la causa più comune di meningite eosinofila, una condizione grave che può portare alla morte o danni permanenti al cervello e ai nervi. Angiostrongyliasis è un'infezione di crescente importanza per la salute pubblica, poiché la globalizzazione contribuisce alla diffusione geografica della malattia.
Angiostrongylus cantonensis é um parasita nematóide (verme) que causa angiostrongilíase, a causa mais comum de meningite eosinofílica no sudeste da Ásia e na bacia do Pacífico.[1]
Angiostrongylus cantonensis é um parasita nematóide (verme) que causa angiostrongilíase, a causa mais comum de meningite eosinofílica no sudeste da Ásia e na bacia do Pacífico.
Angiostrongylus cantonensis là một loại giun ký sinh ở phổi của chuột, đầu tiên được phát hiện trên chuột bởi tại Canton. Ký sinh trùng giun tròn loại Angiostrongylus cantonensis còn gọi là giun mạch hoặc tên đồng nghĩa Parastrongylus cantonensis, theo phân loại ký sinh trung giun sán thì đây là loài giun tròn.
Ký sinh trùng Angiostrongylus cantonensis nhiễm cho người do nhiễm tình cờ qua nhiều phương thức khác nhau, bình thường chúng ta hay gặp ký sinh trên chuột. Nhiễm giun do ăn phải các loại nhuyễn thể hoặc ốc nước ngọt xử lý, chưa nấu chín và đó cũng là các vật chủ trung gian chủ yếu của loài KST này hoặc các loại rau xanh nhiễm ấu trùng trong chất nhờn của các con ốc, con sên hoặc các sinh vật dẹp bám dính trên đất. Ấu trùng di chuyển đến màng não, ký sinh và gây bệnh và có thể phát hiện được trong dịch não tủy. Chúng di hành trong nhu mô não, đôi khi đến mắt, nơi đó chúng tăng lên và gây phản ứng viêm cấp với biểu hiện tăng bạch cầu eosine. Màng não có thể biểu hiện các tổn thương và xuất hiện triệu chứng màng não hoặc vỏ não, các triệu chứng, biến chứng đó liên quan đến các ổ abces tăng nhiễm eosin, xuất huyết và vệt giun chứa các tinh thể Charcot-Leyden xung quanh mô hoặc nốt giun đóng kém chết bên trong. Khi giun gần trưởng thành, chúng di chuyển đến các nhánh động mạch phổi. Ở chuột (vật chủ tự nhiên của loài KST này), các trứng và ấu trùng sinh ra phản ứng viêm ít hơn nhưng ở con người, chu kỳ có thể kết thúc khi giun chết bên trong động mạch phổi.
Trường hợp bệnh viêm màng não-não do A. cantonensis ở người đầu tiên được phát hiện ở một bé trai tại Ðài Loan (Nomura và Lin., 1945), khi đó sáu con giun trong dịch não tủy của bệnh nhi này. Trên người, giun có thể gây viêm não, màng não với sự gia bạch cầu toan tính, hoặc ái tính với mô mắt. Bệnh lưu hành phổ biến ở Viễn Ðông, một số đảo ở Thái Bình Dương, Ðông Nam Á, nhất là Ðài Loan, Nhật Bản, Thái Lan. Theo một nghiên cứu tổng thể của John H.Cross, thuộc khoa Khoa học sức khỏe, đại học y khoa Hebert, Bethesda, Maryland, Hoa Kỳ tổng kết loài ký sinh trùng Angiostrongylus cantonensis phân bố nhiều ở Philippines, Indonesia, Malaysia, Thái Lan,Việt Nam, Đài Loan, Hồng Kông, Nhật Bản, đảo Tahiti, New Caledonia, Papua New Guinea, Australia, Cuba, Puerto Rico, Hawaii. Tính đến năm 2000, tổng số hơn 3.500 trường hợp viêm màng não tăng bạch cầu ái toan do ký sinh trùng này được báo cáo tại trên 30 quốc gia trên thế giới.
Tại Mỹ thì loài ký sinh trùng này tìm thấy trên chuột, các loài nhuyễn thể và một trường hợp được báo cáo từ New Orleans; ở châu Phi (Madagascar) thì A.cantonensis được phát hiện ở chuột. Riêng tại Việt Nam, kể từ năm 1960 thì số trường hợp viêm màng não-não nghi ngờ do A. cantonensis cũng được ghi nhận và báo cáo, đặc biệt là trường hợp bệnh nhân mổ tử thi phát hiện giun này (Phan Trinh và cs., 1974). Từ đó đến nay số ca phát hiện ngày một tăng lên, mỗi năm khoảng gần 70-100 trường hợp được phát hiện trên phạm vi toàn quốc, số ca được phát hiện quá thấp so với số ca được xét nghiệm dương tính đến nhiều lần (mặcdù có tỷ lệ dương tính giả cao), song điều đó có nghĩa là bệnh nhiễm KST này mới chỉ được các thầy thuốc lưu tâm trong 10 năm qua cùng với sự tiến bộ của y học chẩn đoán, đặc biệt lĩnh vực huyết thanh chẩn đoán.
Đặc điểm bệnh nhân nhiễm A.cantonensis là có thể gặp ở mọi lứa tuổi, nhưng thường gặp (58- 76%) trong độ tuổi lao động (15-55 tuổi), trẻ dưới 15 tuổi cũng chiếm tỷ lệ không nhỏ đến 10-24%. Giới nam gặp nhiều hơn nữ qua nhiều báo cáo trong nước và y văn thế giới, chiếm tỷ lệ trên 70%, có lẽ nam giới thường ăn những thức ăn tái, sống, trộn hơn là nữ giới (N.T.Xuân., 2005; H.H.Quang và cs.,2007). Đa số bệnh nhân là dân lao động (70-90%), nông dân và ngư dân chiếm số lớn và điều kiện làm việc của họ tiếp xúc với mầm bệnh (bắt ốc, sò huyết, ốc nhảy, hàu, vẹm đỏ, vẹm xanh, ốc sống). Cách chế biến của họ cũng đơn giản thường ăn sống chấm với hỗn dịch [mù tạt + xì dầu hay tương đen] hoặc thái mỏng trộn gỏi, hấp ăn với gừng, xả,…chưa đủ đảm bảo chết ấu trùng giai đoạn nhiễm.
A.cantonensis ký sinh trong một vài loài ốc sống trên mặt đất (Achatina fulica, loại ốc lớn ở châu Phi), ốc sống dưới nước (Pila spp., Viviparus javanica), hoặc sên (Veronicella alte và siamensis) có thể đóng vai trò vật chủ trung gian cho sự phát triển của ấu trùng L3. Sự tồn tại của các vật chủ trung gian chính được mô tả: trong các loài tôm nước ngọt, cua đất và ếch sống nhờ ăn ốc và sên, ấu trùng vẫn duy trì thể nhiễm (L3)trong một số giai đoạn và có thể nhiễm vào chuột, hoặc con người khi ăn các vật chủ trung gian như Achatina fulica.
Người bị nhiễm do ăn phải ốc, con sên, rau hoặc vật chủ truyền nào đó chưa được nấu chín; ở người, ấu trùng di chuyển đến hệ thần kinh trung ương, ở đó sự phát triển của chúng dừng lại và gây ra viêm não- màng não tăng bạch cầu eosine. Khi chúng đẻ và giải phóng ra ấu trùng giai đoạn 1 (L1), ấu trùng này sẽ di chuyển đếnruột non thông qua đường khoang phế nang, khí quản, hầu và thực quản; rồi ấu trùng đào thải cùng với phân. Ấu trùng L1 nhiễm vào các vật chủ trung gian thứ nhất là các loài nhuyễn thể (ốc và sên), ở đó chúng phát triển thành ấu trùng gây nhiễm giai đoạn ba (L3). Các con chuột bị nhiễm do ăn phải ốc hoặc sên có dính ấu trùng L3, ấu trùng trong chuột sẽ di chuyển từ ruột đến hệ thần kinh trung ương và trưởng thành tại đó trải qua 2 giai đoạn phát triển trong thời gian 2 đến 3 tuần. Tiếp đến các con giun trưởng thành đến khoang dưới nhện, vào trong hệ tĩnh mạch, vào động mạch phổi và trưởng thành đến giai đoạn hoàn chỉnh. Ấu trùng có thể phát hiện ở phân chuột trong vòng 40-60 ngày sau nhiễm.
Cắt con giun A.cantonensis trong khoang dưới nhện với tổ chức viêm và xuất huyết (khi nhuộm hematoxylin và eosin), bệnh sinh do A.cantonensis tùy dựa vào tổn thương trực tiếp gây ra bởi ấu trùng di chuyển và giun còn non (dài 7-13mm x 100-260 µm) và phản ứng u hạt viêm.
Xét nghiệm mô học cho thấy lát cắt của giun bao bọc xung quanh bởi các tế bào viêm (bao gồm bạch cầu neutrophil và eosinophil), sung huyết mao mạch, xuất huyết khoang dưới nhện và dưới màng cứng, hoại tử ổ tại chỗ và xuất huyết trong não. Mặt cắt các con giun non trưởng thành của A. cantonensis trong não không có đáp ứng viêm; mặt cắt phẫu tích giun trưởng thành còn non, tổn thương ở phổi của A.cantonensis hoặc trong não cũng được nhìn thấy rõ qua nhuộm hematoxylin và eosin; một vài giun trưởng thành, con cái và đực có thể nằm bên trong cùng mao mạch phổi.
Bệnh do Angiostrongylus cantonensis có thời gian ủ bệnh từ 1-5 tuần (trung bình 2 tuần), hoặc 15-17 ngày hoặc chỉ 11-13 ngày, triệu chứng bệnh thường có sốt, nhức đầu là hai triệu chứng hay gặp nhất (đau đầu khu trú chủ yếu vùng chẩm và thái dương), cứng gáy, buồn nôn, nôn mửa, sốt thường nhẹ (37.8-390C), phát ban đỏ, ngứa, đau bụng và một số triệu chứng toàn thân; sốt có khi không rõ ràng, nhiều trường hợp hết sốt khi nhập viện mặc dù chưa điều trị bất kỳ một loại thuốc đặc hiệu. Đây là bệnh viêm màng não (do ký sinh trùng) nhưng dấu hiệu màng não khá ít, chỉ khoảng 30-48% số bệnh nhân. Bệnh nhân thường nhập viện trễ, trên 50% số ca đến nhập viện khi bệnh đã kéo dài hơn 2 tuần với một số chẩn đoán trước đó khá đa dạng là đau đầu do viêm mạch Horton, viêm màng não mủ, viêm não do virus, u não,… Tử vong do bệnh nhiễm KST này rất hiếm gặp.
Triệu chứng hệ thần kinh do A.cantonensis thường gây ra một số triệu chứng màng não, liệt một số dây thần kinh sọ não như dây III, IV, VI, VII, nhưng dấu thần kinh định vị chiếm tỷ lệ cao là ở liệt dây thần kinh sọ não VI, VII thường gặp nhất, 7-12% bệnh nhân có biểu hiện triệu chứng tổn thương tủy sống (yếu, liệt một hoặc 2 chi dưới, rối loạn cơ vòng). Tỷ lệ bệnh nhân có rối loạn tri giác cũng cao, nhưng mức độ rối loạn tri giác thường không nghiêm trọng, các triệu chứng khác như đau cơ, rối loạn cảm giác, hồng ban cũng khá thường gặp với tỷ lệ lần lượt 14%; 17% và 8%; dị cảm ở mặt, đau, yếu chi là các dấu chứng cũng thường gặp.
Phần lớn các trường hợp nhiễm Angiostrongylus cantonensis có hình ảnh tổn thương khá rõ, song không điển hình cho một bệnh lý nào, tuy nhiên nếu kết hợp một số xét nghiệm khác như công thức bạch cầu, huyết thanh miễn dịch có thể cho chẩn đoán thấu đáo hơn. Trên hình ảnh lát cắt của phim chụp CT_Scanner hoặc MRI cho các hình ảnh nốt canxi hóa, vôi hóa trong nhu mô não, rãnh não,…
Thể bệnh ký sinh hoặc di chuyển trong hệ thần kinh và sang bộ phận thị giác, ở mắt có hiện diện của giun trưởng thành còn non A. cantonensis bên trong buồng trước của nhãn cầu đã được mô tả, hoặc có giảm thị lực, đau nhức hố mắt, sụp mi hoặc sa mi mắt (blepharospasm), viêm mống mắt thể mi (iridocyclitis) và tăng co giật nhãn cầu trên một số bệnh nhân. Triệu chứng ở phổi do A.cantonensis là triệu chứng khá điển hình phổ biến nhưng hiếm, một vài giun có thể di chuyển đến phổi gây viêm phổi nặng, dạng abces ổ trong nhu mô phổi, xuất tiết và xuất huyết.
Khai thác bệnh sử một số nhóm nghiên cứu ghi nhận bệnh nhân mắc loại KST này có liên quan đến bệnh là có tiền sử ăn ốc sống hoặc các chế phẩm tái sống từ ốc, hoặc ăn các loại rau thủy sinh dính chất nhớt từ ốc (52-64%) trước đó. Tuy nhiên, đây có thể là tập quán ăn uống và thói quen ăn uống của học nên chỉ xếp vào loại có nguy cơ. Bệnh nhân nhập viện nhiều nhất vào 3 tháng cuối năm ở các quốc gia có khí hậu nóng ẩm, thời điểm này là 3 tháng cuối mùa mưa, ốc cũng như các loài nghuyễn thể, thực vật thủy sinh, phát triển mạnh nhất, con người khi đó lại sử dụng nhiều rau, ốc, tôm, cá làm thức ăn chính và nếu không được nấu chín thì dễ dàng nhiễm bệnh.
Chẩn đoán xét nghiệm ký sinh trùng A.cantonensis dựa vào sự có mặt loại bạch cầu eosine trong dịch não tủy tăng cao, có kèm hay không tăng lympho bào (500 - 5.000 tế bào/mm3, với 20 - 90% là eosin), nhất là những trường hợp viêm màng não đến muộn, tăng proteine và giảm nhẹ glucose trong dịch não tủy. Hai yếu tố đóng góp rất quan trọng trong chẩn đoán bệnh do Angiostrongyliasis là tiền sử có ăn các loại vật chủ trung gian nhiễm bệnh chính trong vùngvà bằng chứng về kháng nguyên hoặc kháng thể trong dịch não tủy hoặc trong mắt. Khoảng 27% số ca nhiễm giun A.cantonensis, người ta phát hiện tinh thể Charcot-Leyden có mặt trong dịch não tủy, cùng tăng bạch cầu, với tỷ lệ eosin ưu thế (> 10%), chẩn đoán có thể xác định bởi xét nghiệm huyết thanh miễn dịch như IF, EIA hoặc ELISA.
Đa số trường hợp viêm màng não-não nghi do giun A.cantonensis khó chẩn đoán chắc chắn vì không thể bắt được giun làm chẩn đoán chuẩn vàng, có lẽ một xét nghiệm có độ đặc hiệu và độ chính xác cao là cần thiết để xác định chẩn đoán nguyên nhân, rất tiếc điều này vẫn đang ở phía trước và trong giai đoạn nghiên cứu; thực tiễn lâm sàng bệnh do A. cantonensis được xác định khi bắt được giun trong dịch não tủy, mà điều này lại hiếm khi thực hiện được.
Vì vậy, trên thế giới, người ta đã nghiên cứu nhiều kỹ thuật chẩn đoán gián tiếp nhưng đặc hiệu như kỹ thuật huyết thanh miễn dịch (phản ứng kết tủa, ngưng kết hồng cầu thụ động, ngưng kết latex, miễn dịch hấp thụ liên kết men, miễn dịch phóng xạ, khuếch tán gel kép,…). Trong số đó, kỹ thuật miễn dịch hấp phụ men (ELISA) tỏ ra thích hợp hơn trong chẩn đoán các bệnh KST thường quy tại các phòng xét nghiệm (do ít tốn sinh phẩm, hoá chất, thao tác đơn giản và có thể tự động hoá được). Ngoài ra, kỹ thuậy này có thể phát hiện được kháng thể (Ab-ELISA) và kháng nguyên lưu hành (Ag-ELISA).
Với mục đích góp phần chẩn đoán bệnh nhiễm ký sinh trùng Angiostrongylus cantonensis ở người, nhiều kit ELISA ra đời để phát hiện ra kháng thể đặc hiệu với kháng nguyên A. cantonensis (specific Ab-Ag), kỹ thuật miễn dịch hấp thụ men (ELISA) được nghiên cứu để chẩn đoán rất nhiều bệnh do ký sinh trùng, trong đó có bệnh A. cantonensis ở người. Kháng nguyên A. cantonensis ở nồng độ 3 ng/ml gắn kết với kháng thể có trong huyết thanh chứng (+) tạo thành phức hợp kháng nguyên-kháng thể (Ag-Ab). Phức hợp này được phát hiện bởi cộng hợp IgG thỏ kháng IgG người có gắn peroxydase với sự hiện diện của chất nền.
Hiệu giá kháng thể của các trường hợp nhiễm Angiostrongylus cantonensis được ghi nhận từ 1/400-1/ 6400 (tùy thuộc vào từng kit ELISA của các hàng khác nhau Song song với thử nghiệm, người ta cũng làm với mẫu huyết thanh của người tình nguyện khoẻ mạnh có hiệu giá kháng thể dao động từ 1/50-1/200. Phản ứng chéo (cross-reaction) cũng được ghi nhận giữa A. cantonensis với Gnathostoma spinigerum, sán lá phổi Paragonimus sp. và giun đũa chó Toxocara canis theo một số nghiên cứuy văn trong nước và thế giới.
Dù thế nào chăng nữa trong thời gian đến, cần có nghiên cứu nhân rộng đánh giá độ nhạy, độ chính xác, độ đặc hiệu và độ tương đồng (Kappa’ test) của ELISA với một số xét nghiệm cao cấp hơn. Chẩn đoán dựa vào kỹ thuật sinh học phân tử PCR cũng cho phép xác định sự có mặt của ký sinh trùng A.cantonensis trong nhu mô não, hoặc một số xét nghiệm miễn dịch khác được áp dụng trong nghiên cứu, song kết quả không đáng tin cậy trong chẩn đoán xác định bệnh như IFA, IHA, CIE.
Đến thời điểm này, chưa có loại thuốc điều trị nào tỏ ra có hiệu quả chữa khỏi hoàn toàn bệnh viêm màng não do giun A.cantonensis, ngay cả các thuốc chống giun sán thông thường cũng không được khuyến cáo là chắc chắn. Một số nghiên cứu trong y văn và thực hành lâm sàng cho biết một số phác đồ điều trị tỏ ra có hiệu quả phần nào, đặc biệt chú ý di chứng thần kinh sau điều trị vẫn còn đến khi đã xuất viện.Do vậy, quản lý và giám sát điều trị ca bệnh đặc biệt về mặt chăm sóc theo chuyên khoa thần kinh, chú ý tránh các biến chứng nhiễm trùng.
Phác đồ điều trị bằng albendazole, thời gian trung bình là 14-21 ngày, có hoặc không kèm theo dùng corticoisteroides, nếu có thì rút ngắn thời gian điều trị còn 1 tuần. kết quả điều trị khoảng chừng 30-45%, song vẫn còn một số dấu chứng thần kinh định vị, rối loạn trị giác, nhức đầu,…; có thể thêm thuốc giảm đau, chống phù não,… Phác đồ Albendazole và prednisolone trong 2 tuần cũng cho hiệu quả và an toàn cao (trên 35 bệnh nhân bị VMNTBCAT);
Phác đồ với Mebendazole và/hoặc Interleukin hiện đang thử nghiệm điều trị trên chuột, bước đầu cho hiệu quả cao với 100 mg x 2 lần. ngày trong 5 ngày; Nghệ là sản phẩm tự nhiên có tác dụng chống viêm, chống oxy hóa, và chống ung thư, gần đây người ta ghi nhận có tác dụng giảm triệu chứng viêm màng não do tăng bạch cầu eosin, kết quả cho biết nghệ có thể giết chết ấu trùng của A,cantonensis, bạch cầu eosin giảm nhanh chóng.
Vì bệnh do A.cantonensis có thể dễ dàng loại bỏ bằng cách nấu chín các loại thức ăn từ thực phẩm rau thủy sinh hoặc động vật nhuyễn thể, các biện pháp truyền thông giáo dục sức khỏe là ưu tiên triển khai cho chiến lược phòng bệnh, tránh những hậu quả và di chứng nghiêm trọng cho cộng đồng. Sơ đồ bên có thể cho phép chúng ta hình dung được biện pháp nào để cắt đứt các khâu lan truyền bệnh do loài ký sinh trùng nguy hiểm này.
Angiostrongylus cantonensis là một loại giun ký sinh ở phổi của chuột, đầu tiên được phát hiện trên chuột bởi tại Canton. Ký sinh trùng giun tròn loại Angiostrongylus cantonensis còn gọi là giun mạch hoặc tên đồng nghĩa Parastrongylus cantonensis, theo phân loại ký sinh trung giun sán thì đây là loài giun tròn.
廣東住血線蟲(學名: Angiostrongylus cantonensis)是住血線蟲屬(Angiostrongylus)的一個物種,因為生活週期中會寄生在老鼠肺部,所以又叫鼠肺蟲(英语:Rat lungworm),可引起的病名稱為广州管圆线虫病,病徵包括嗜伊紅性腦膜腦炎和腦膜炎[2]。舊屬後圓線蟲科,今屬後圓線蟲總科的住血線蟲科。屬寄生蟲
本物種由中國寄生蟲學家陳心陶於1935年首度在廣東省的鼠隻發現[1];1945年日本殖民台灣時期由野村和林兩人於台南縣在一名15歲日本人的腦脊髓液裡發現,為首次在人體所發現。他們留意病人曾經吃過未經煮熟的食物,而這些食物很可能為鼠隻所感染。1955年,Mackerass & Sanders (1955)確認了這種線蟲在鼠隻體內的生命週期,並以腹足綱物種作為中間宿主,透過血液、腦部及肺部傳染鼠隻。
1985年6月27日,台灣知名醬油廠金蘭食品董事長鍾秋桂一家因生食非洲大蝸牛(Lissachatina fulica)而感染廣東住血線蟲,導致鍾秋桂夫婦及長子鍾德富、母親鍾林腰共四人死亡,次子鍾德尚臥床十年後也不治逝世,全家僅當時身在美國的三子鍾德亨倖存[2]。
2013年,美國佛羅里達州首度發現這種線蟲透過非洲大蝸牛來散播,使人關注這物種肆瘧的範圍在擴展[3]。
在大鼠肺動脈所產下的卵,於微血管中孵化成第一期幼蟲,經氣管食道在糞便排出體外。
軟體動物(例如:非洲大蝸牛)可攝食入第一期幼蟲,在體內發育成第三期幼蟲,人或老鼠(尤其是大鼠)吃下軟體動物或受汙染的飲水或生菜而得病。在囓齒類,幼蟲穿過腸管進門脈循環後,移至宿主腦部經脫皮兩次,回到宿主肺臟。 在人體中,幼蟲進入腦部不再發育。
在動物的臨床症狀:輕度感染不顯性,大鼠可見肢體無力,步伐障礙、呼吸促迫,發紺、流鼻血; 血樣淚水。嚴重時,會昏睡、腦僵直、麻痺、死亡。在人臨床症狀常見有腦炎、腦膜炎、噁心、嘔心、發燒、角膜炎 、虹膜炎、視網膜水腫、嚴重會昏睡及死亡。
MRI定位儀雷射可觀察患部;腰椎穿刺抽取腦脊髓液、檢測嗜酸性球增加數量亦可作為診斷,用血清以及腦脊髓液進行ELISA抗原-抗體測試。
除了撲滅鼠類外,應該要移除其第一中間宿主,像是螺蛳、非洲大蝸牛等,食物應該確實煮熟,及在-15℃下冷凍保存達24小時以上。
不食用未煮熟之螺蛳、蛞蝓、淡水明蝦、生菜等中間宿主;要注意非洲大蝸牛的接觸史,以防其糞便或是黏液中帶有蟲卵,並且應全面清除;也需要注意儲蟲宿主的大鼠是否造成排泄物汙染食物的可能。此防治措施施實背景以台灣為主,其他地方應參考當地可能的野生動物,而修正公衛策略。
人類感染發生於整個大洋洲(特別是夏威夷、薩摩亞群島、索羅門群島、巴布亞新幾內亞、印尼、菲律賓和澳大利亞北部);東南亞(特別是泰國、台灣、日本以及印度);一些感染曾報告於非洲和中南美洲,亦有報告存在美國紐奧良和路易斯安那。
廣東住血線蟲(學名: Angiostrongylus cantonensis)是住血線蟲屬(Angiostrongylus)的一個物種,因為生活週期中會寄生在老鼠肺部,所以又叫鼠肺蟲(英语:Rat lungworm),可引起的病名稱為广州管圆线虫病,病徵包括嗜伊紅性腦膜腦炎和腦膜炎。舊屬後圓線蟲科,今屬後圓線蟲總科的住血線蟲科。屬寄生蟲